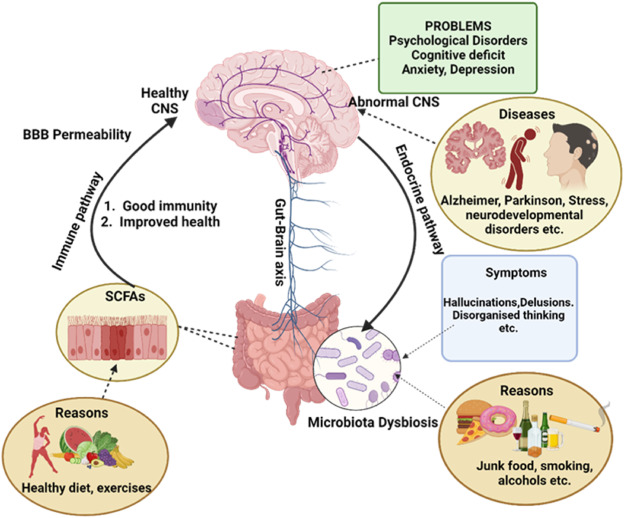
Die menschliche Gastrointestinalmikrobiota (GI-Mikrobiota) – das komplexe Ökosystem aus Billionen von Mikroorganismen im Darm – spielt eine zentrale Rolle für Gesundheit und Krankheit. Über die letzten Jahre hat sich gezeigt, dass diese Mikroorganismen weit mehr tun, als nur Nahrung zu verdauen: Sie beeinflussen das Immunsystem, die metabolische Funktion und sogar das Gehirn. Eine besonders spannende Verbindung ist die sogenannte Darm-Hirn-Achse, ein bidirektionales Kommunikationssystem zwischen dem zentralen Nervensystem (ZNS) und dem enterischen Nervensystem (ENS), das auch das Immunsystem aktiv mit einbezieht.
GI-Mikrobiota:
Die GI-Mikrobiota umfasst Bakterien, Viren, Pilze und Archaeen, wobei Bakterien wie Bacteroides, Firmicutes, Actinobacteria und Proteobacteria dominieren. Diese Mikroorganismen entwickeln sich ab der Geburt und werden durch Ernährung, Antibiotika, Lebensstil und Umwelt geprägt. Sie leisten essentielle Beiträge zur:
-
Verdauung komplexer Kohlenhydrate
-
Synthese von Vitaminen (z. B. B12, K)
-
Modulation des Immunsystems
-
Schutz vor pathogenen Keimen (Kolonisierungsresistenz)
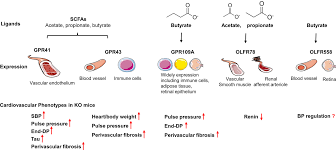
Mikrobielle Metabolite:
Ein zentraler Mechanismus, über den die Mikrobiota mit dem Wirt interagiert, ist die Produktion von Metaboliten, darunter:
-
Kurzkettige Fettsäuren (SCFAs) wie Butyrat, Acetat und Propionat
-
Tryptophan-Metabolite wie Indole, Kynurenin und Serotonin
-
Gallensäure-Derivate und mikrobielle Neurotransmitter (z. B. GABA, Dopamin)
Diese Metaboliten agieren nicht nur lokal im Darm, sondern zirkulieren im gesamten Körper und beeinflussen systemische Prozesse, einschließlich Immun- und Nervenfunktionen.
GI-Mikrobiota und das Immunsystem:
Etwa 70–80 % der Immunzellen befinden sich im Darm. Die Interaktion zwischen der GI-Mikrobiota und dem Immunsystem ist essenziell für die Entwicklung und Homöostase der Immunantwort. Wichtige Aspekte dieser Interaktion sind:
-
Toleranzentwicklung: Darmbakterien fördern die Ausbildung regulatorischer T-Zellen (Tregs), die überschießende Immunantworten verhindern.
-
Barrierefunktion: Butyrat fördert die Bildung von tight junctions in der Darmschleimhaut, verhindert Leaky-Gut-Syndrome und senkt die Immunaktivierung durch mikrobielle Produkte.
-
Pattern Recognition Receptors (PRRs): Rezeptoren wie Toll-like-Rezeptoren (TLRs) erkennen mikrobielle Signale (z. B. Lipopolysaccharide) und modulieren daraufhin Immunreaktionen.
-
Zytokinregulation: Mikrobielle Signale beeinflussen das Gleichgewicht pro- und antiinflammatorischer Zytokine wie IL-10, IL-6, TNF-α und IFN-γ.
-
Systemische Wirkung: Eine gestörte Mikrobiota kann systemische Entzündung fördern – ein relevanter Mechanismus bei neuroinflammatorischen Erkrankungen.
Die Darm-Hirn-Achse:
Die Darm-Hirn-Achse ist keine rein neuronale Verbindung, sondern ein komplexes Netzwerk, das auch das Immunsystem aktiv einbindet:
Neuronal: über den Vagusnerv, der Signale vom Darm zum Gehirn transportiert
Endokrin: durch Hormone und neuroaktive Substanzen
Immunologisch: durch Zytokine, Immunzellmigration und entzündliche Signale
Metabolitär: durch mikrobiell produzierte Stoffwechselprodukte
Besonders neuroinflammatorische Prozesse, die durch Mikrobiota-induzierte Zytokinveränderungen entstehen, stehen im Verdacht, neurologische Störungen wie Depressionen, Alzheimer oder Multiple Sklerose mitzuverursachen oder zu verschlimmern.
Die Rolle von Entzündungen
Chronische, niedriggradige Entzündungen („low-grade inflammation“) – häufig eine Folge gestörter Darmmikrobiota – gelten als Risikofaktor für:
-
Depressionen (über Aktivierung der HPA-Achse und Tryptophan-Stoffwechsel)
-
Neurodegeneration (z. B. Mikroglia-Aktivierung durch periphere Zytokine)
-
Autismus-Spektrum-Störungen (über Immunmodulation in der Frühentwicklung)
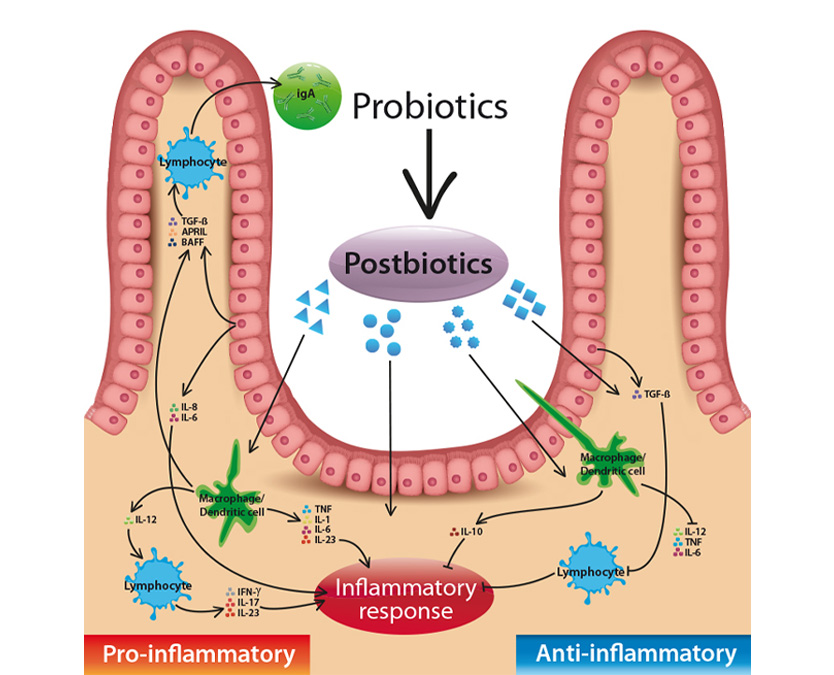
Psychobiotika und Immunmodulation
Einige Psychobiotika zeigen nicht nur neuroaktive, sondern auch immunmodulatorische Effekte. Bifidobacterium infantis kann z. B. IL-10 erhöhen, während Lactobacillus casei entzündliche Marker senkt. Dies eröffnet neue Therapieansätze für psychische Erkrankungen mit immunologischer Komponente.
Summary
Die Interaktion zwischen GI-Mikrobiota, Metaboliten, Immunsystem und dem Gehirn ist hochkomplex, aber essenziell für die ganzheitliche Gesundheit. Die Darm-Hirn-Achse funktioniert nur im Gleichgewicht – und das wird maßgeblich durch die Mikrobiota geprägt. Der Einbezug des Immunsystems als Vermittler zwischen Darm und Gehirn ist ein zentrales Element dieses Netzwerks und könnte in Zukunft Schlüsselrolle bei der Behandlung von neuropsychiatrischen und autoimmunologischen Erkrankungen spielen.
Your content goes here. Edit or remove this text inline or in the module Content settings. You can also style every aspect of this content in the module Design settings and even apply custom CSS to this text in the module Advanced settings.